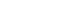ut Rucaparib camsylate (w)
Cellulose microcristalline (H)
Carboxyméthylamidon sodique (type A) (H)
Silice colloïdale anhydre (H)
Magnésium stéarate (H)
Alcool polyvinylique (H)
Macrogol 4000 (H)
Talc (H)
Titane dioxyde (E171) (H)
Oxyde de fer jaune (E172) (H)
corresp.: Sodium max. (1.8 mg) (H)
pro compr. obduct.
Antinéoplasiques > Autres antinéoplasiques > Inhibiteurs de PARP
>18 ans: 600 mg 2×/j. à intervalle de 12 h jusqu'à progression de la maladie.
• Au moins deux chimiothérapies préalables à base de platine, la dernière de ces chimiothérapies à base de platine devant remplir les critères suivants:
o les patientes doivent avoir reçu au moins 4 cycles de la thérapie à base de platine, après le dernier traitement, la patiente doit avoir présenté un CA-125 < ULN
• Pas de traitement/traitement d’entretien préalable avec des inhibiteurs de PARP. Une exception à cela est un changement lié à la tolérance dans la même ligne de traitement à un autre inhibiteur de PARP.
Le traitement est poursuivi jusqu’à progression de la maladie.
Les traitements en association ou séquentiels tels que bévacizumab et rucaparib ou des traitements immuno-oncologiques et le rucaparib ainsi que la reprise de traitements sur des lignes de traitement supérieures après une nouvelle rechute ne sont pas remboursés.
Durant les 24 premiers mois, les montants remboursés sont ceux figurant sur la LS. Pour un traitement d’une durée supérieure (à partir de 25 mois), le titulaire de l’autorisation rembourse 50% du prix départ usine pour l’achat de toute boîte supplémentaire de Rubraca sur demande de l’assureur-maladie auprès duquel l’assuré était assuré au moment de l’achat. La taxe sur la valeur ajoutée ne peut pas être exigée en sus de ce montant. La demande de remboursement doit intervenir en règle générale dans les 6 mois qui suivent l’administration.
• Au moins deux chimiothérapies préalables à base de platine, la dernière de ces chimiothérapies à base de platine devant remplir les critères suivants:
o les patientes doivent avoir reçu au moins 4 cycles de la thérapie à base de platine, après le dernier traitement, la patiente doit avoir présenté un CA-125 < ULN
• Pas de traitement/traitement d’entretien préalable avec des inhibiteurs de PARP. Une exception à cela est un changement lié à la tolérance dans la même ligne de traitement à un autre inhibiteur de PARP.
Le traitement est poursuivi jusqu’à progression de la maladie.
Les traitements en association ou séquentiels tels que bévacizumab et rucaparib ou des traitements immuno-oncologiques et le rucaparib ainsi que la reprise de traitements sur des lignes de traitement supérieures après une nouvelle rechute ne sont pas remboursés.
Durant les 24 premiers mois, les montants remboursés sont ceux figurant sur la LS. Pour un traitement d’une durée supérieure (à partir de 25 mois), le titulaire de l’autorisation rembourse 50% du prix départ usine pour l’achat de toute boîte supplémentaire de Rubraca sur demande de l’assureur-maladie auprès duquel l’assuré était assuré au moment de l’achat. La taxe sur la valeur ajoutée ne peut pas être exigée en sus de ce montant. La demande de remboursement doit intervenir en règle générale dans les 6 mois qui suivent l’administration.
Contacts