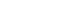ut Acoramidis hydrochlorid (w)
Cellulose, mikrokristalline (H)
Croscarmellose natrium (H)
corresp.: Natrium (3.24 mg) (H)
Siliciumdioxid hydrat (H)
Magnesium stearat (H)
Überzug:
Macrogol-Poly(vinylalkohol)-Pfropfcopolymer (H)
Talkum (H)
Titandioxid (E171) (H)
Glycerolmonocaprylocaprat (H)
Polyvinylalkohol (H)
Drucktinte
Eisenoxid schwarz (E172) (H)
Propylenglycol (H)
Hypromellose (H)
pro compr. obduct.
Kardiaka > Transthyretin-Amyloidose

hATTR-Patienten mit primär polyneuropathischer Manifestation sind von der Vergütung einer Therapie mit BEYONTTRA ausgeschlossen.
Die Diagnosestellung der kardialen ATTR-Amyloidose hat wie folgt zu erfolgen: Positive Knochenszintigraphie (Perugini Grad 2-3), Echokardiographie (z.B. typisches Strain-Muster), bei gleichzeitigem Ausschluss einer AL-Amyloidose (Ausschluss einer monoklonalen Gammopathie mittels Messung der freien Leichtketten im Serum, sowie Serum- und Urin-Immunfixationselektrophorese). Im Fall eines unklaren/unsicheren Szintigraphiebefundes oder/und keines eindeutigen Ausschlusses der AL-Amyloidose oder/und eines nicht eindeutigen Befundes in der kardialen Bildgebung ist eine Biopsie mit histologischem Nachweis von Transthyretin-Amyloid notwendig.
Vor Therapiebeginn:
Die Diagnosestellung der kardialen Transthyretin-Amyloidose, die Verschreibung und die Überwachung der Therapie mit BEYONTTRA kann nur durch ein spezialisiertes, interdisziplinär zusammengesetztes Ärzteteam in einer zertifizierten kardiologischen Weiterbildungsstätte der Kategorie A erfolgen.
Vor Therapiebeginn muss eine Kostengutsprache des Krankenversicherers nach vorgängiger Konsultation des Vertrauensarztes eingeholt werden.
Bevor die Therapie eingeleitet werden kann, ist der Patient über die Vergütungskriterien (inkl. Therapieabbruchkriterien) schriftlich aufzuklären.
Folgende Kriterien müssen kumulativ erfüllt sein für einen Therapiebeginn mit BEYONTTRA:
– NT-pro BNP-Konzentration ≥ 300pg/ml
– Distanz gemäss 6-Minuten-Gehtest ≥150 Meter oder äquivalentes Resultat aus einer ergometrischen Bestimmung
– eine Lebenserwartung von mindestens 2 Jahren
BEYONTTRA wird nicht vergütet bei Patienten mit Vorgeschichte einer Leber- oder Herztransplantation, bei Patienten, denen «mechanic assist devices» (LVAD, RVAD, BiVAD) implantiert wurde oder bei Patienten mit Niereninsuffizienz (glomeruläre Filtrationsrate < 25 mL/Min./1.73 m2).
BEYONTTRA darf nicht mit anderen spezifischen Arzneimitteln zur Behandlung der Transthyretin-Amyloidose (z.B. TTR-Stabilisatoren, TTR-Gen Silencer) kombiniert werden. BEYONTTRA wird nicht vergütet, falls eine vorherige ATTR-CM Therapie mit einem TTR-Stabilisator aufgrund der Therapieabbruchkriterien gestoppt werden musste.
Therapieevaluation und Dokumentation:
Dokumentation von NYHA-Stadium, NT-proBNP, 6-Minuten-Gehtest oder Ergometrie, Herzinsuffizienz-bedingten Hospitalisationen und Diuretika-Verbrauch vor Therapiebeginn und regelmässig während der Behandlung mit BEYONTTRA (zumindest alle 6 Monate) sowie von transthorakaler Echokardiographie (zumindest alle 12 Monate). Bei Patienten, die während den vorangegangenen 12 Monaten keine Verschlechterung in einem der Therapiestoppkriterien zeigten, kann die Evaluation alle 12 Monate durchgeführt werden.
Therapieabbruch:
Die Therapie ist abzubrechen bei:
– ATTR-CM bedingter substanzieller klinischer Verschlechterung während 6 Monaten (z.B. rezidivierende Hospitalisationen aufgrund kardialer Dekompensation)
– ATTR-CM bedingter klinisch relevanter sinkender Leistungsfähigkeit während 6 Monaten in Kombination mit NT-proBNP Anstieg und erhöhtem Diuretika-Verbrauch
– anhaltender schwerer Herzinsuffizienz (NYHA III oder IV) über einen Zeitraum von mindestens 6 Monaten trotz optimaler leitliniengerechter Therapie
– klinisch relevante Verringerung der Gehdistanz (6-Minuten-Gehtest oder äquivalentes Resultat aus einer ergometrischen Bestimmung)
– Durchführung einer Herz- oder Lebertransplantation
– Implantierung von «mechanic assist devices» (LVAD, RVAD, BiVAD)
Pro Kalenderjahr ist dem BAG durch die Referenzzentren die Anzahl der mit BEYONTTRA behandelten Patientinnen und Patienten zu melden, wobei zwischen neu therapierten und bereits in Therapie befindlichen Patientinnen und Patienten zu unterscheiden ist. Die Angaben sind dem BAG innert 4 Monaten nach Stichdatum (31. Dezember) direkt an office@eak-sl.admin.ch zu melden.
Die Zulassungsinhaberin Bayer AG erstattet nach Aufforderung durch denjenigen Krankenversicherer, bei dem die versicherte Person zum Zeitpunkt des Bezugs versichert war, für jede bezogene Packung BEYONTTRA einen festgelegten Betrag des Fabrikabgabepreises zurück. Sie gibt dem Krankenversicherer die Höhe der Rückerstattung bekannt. Die Mehrwertsteuer kann nicht zusätzlich zu diesem Anteil des Fabrikabgabepreises zurückgefordert werden. Die Aufforderung zur Rückerstattung soll ab dem Zeitpunkt der Verabreichung erfolgen.
Folgender Code ist an den Krankenversicherer zu übermitteln: 21994.01
Kontaktmöglichkeiten